

پیش از آغاز موضوع بحث لازم است تا برخی اصلاحات اساسی مورد استفاده در متن تعریف شوند.
قابل ذکر است که بارزترین ویژگی قارچهای رودهای عملکردهای خارج رودهای آنهاست. بررسیهایی که در این زمینه صورت گرفته است حاکی از اهمیت قارچهای روده در تنظیم عملکردهای روده، ریه، کبد، کلیه، پانکراس و مغز است.
با ظهور تکنیکهای جدید در دهه گذشته شاهد انفجاری از توجه به مطالعه میکروبیوم انسانی بودهایم. محققان ریه به طور طبیعی به میکروبهایی که در ریه زندگی میکنند علاقهمند هستند. با این حال، نقش میکروبیوتای روده ممکن است حتی مهمتر از میکروبیوتای ریه در برخی از بیماریهای ریوی باشد.
اگرچه امروزه مشخص شده است که هر سطحی از بدن، از ریهها تا کره چشم، دارای یک میکروبیوم است، اکثریت قریب به اتفاق تنوع زیستی میکروبی در محیط غنی از مواد مغذی دستگاه گوارش یافت میشود. اگر میکروبیوتا به عنوان یک اکوسیستم در نظر گرفته شود، ریههای فقیر از مواد مغذی مانند یک بیابان هستند، اما رودههای غنی از مواد مغذی مانند یک جنگل بارانی هستند.
در واقع، میکروبیوتای روده دارای پیچیدگی بیولوژیکی خاصی است که احتمالاً از پیچیدگی بدن انسان فراتر میرود. تعداد سلولهای بیشتر و محصولات ژنی منحصر به فرد بیشتری در میکروبیوم روده نسبت به تمام سلولهای بومی بدن انسان در کنار هم وجود دارد. این میکروبهای رودهای اکوسیستمی از ارگانیسمها را تشکیل میدهند که با یکدیگر همزیستی و رقابت دارند و همه اینها در مجرای روده اتفاق میافتد که اساساً یک لوله 8 متری است که برای جذب متابولیتها طراحی شده است. مجرای روده همچنین حاوی سلولهای ایمنی میزبان است که حس میکنند و به آنچه در داخل آن اتفاق میافتد پاسخ میدهند.
مفهوم محور روده-ریه بیان میکند که تغییرات میکروبیاتای روده ممکن است تأثیر عمیقی بر بیماری ریه داشته باشد. میکروبها ممکن است توسط سلولهای ایمنی میزبان شناسایی شوند که منجر به آزادسازی سیتوکین سیستمی میشود که جذب سیستم گردش خون میشوند و مستقیماً عملکرد ریه را تغییر میدهند.
رابطه متقابل بین میکروبیوتای روده و ریه در بیماریهای شایع ریوی
یافتههای در حال ظهور نشان میدهند که یک رابطهی متقابل حیاتی بین میکروبیای روده و ریهها وجود دارد که به عنوان محور روده-ریه شناخته میشود. اختلالات روده در بیماریهای ریوی از جمله آلرژی، آسم، بیماری مزمن انسدادی ریه، فیبروز سیستیک و سرطان ریه با مطالعات گسترده مشاهده شده است. بررسی چگونگی تأثیر میکروبیای روده بر سایر اندامها در سالهای اخیر بسیار مورد توجه است. اگرچه به طور کامل مشخص نشده است که آیا این اختلال علت یا اثر بیماریهای ریوی است، تغییرات در گونههای میکروبی روده و متابولیتها با تغییرات در پاسخهای ایمنی و التهاب و همچنین ایجاد و پیشرفت بیماری در ریهها مرتبط است.
هر کس یک ترکیب میکروبی منحصر به فرد دارد. هنگامی که میکروبیوتا به گونهای تغییر کند که تأثیر منفی بر بدن داشته باشند، دیسبیوز نامیده میشود. دیسبیوز مانند عفونت رودهای نیست زیرا احتمالاً میتواند سالها بیصدا و بدون هیچ علامتی رخ دهد.
رودهها علاوه بر اینکه حاوی باکتری هستند، دارای جامعهای از قارچهای مشترک هستند. بسیاری از قارچهایی که هنگام استنشاق در آسم مهم هستند، مانند آسپرژیلوس، پنیسیلیوم یا آلترناریا، به عنوان اجزای مایکوبیوتا روده انسان شناسایی شدهاند. تحقیقات نشان داده است که دیسبیوز قارچی روده شدت آسم را در مدلهای حیوانی افزایش میدهد. گسترش قارچهای منتخب مرتبط با دیسبیوز در رودهها، شدت آسم را بدون هیچگونه قارچ قابل تشخیصی در ریهها افزایش میدهد، که نشاندهنده ارتباط متقاطع محور روده-ریه بین روده و ریه است. این اثر در همه گونههای قارچ مشاهده نمیشود. برخی التهاب آسم را بدتر میکنند، اما برخی دیگر به نظر میرسد هیچ تأثیری ندارند یا حتی ممکن است اثر حفاظتی هم داشته باشند. به نظر میرسد استفاده بیش از حد از آنتیبیوتیکهای طیف گسترده جوامع باکتریایی را مختل میکند و ممکن است یک عامل خطر کلیدی برای ایجاد دیسبیوز قارچی باشد.
میکروبهایی که هم در روده و هم در ریه زندگی میکنند به شیوهای متقابل با میزبان در تعامل هستند. آنها از یک ریزمحیط پایدار غنی از مواد مغذی بهره میبرند و همچنین عملکردهای مهمی مانند تخمیر اجزای غذایی را انجام میدهند. شواهد فزاینده نقش حیاتی و سازنده میکروبها و متابولیتهای آنها را برای حفظ هموستاز سیستم ایمنی نشان میدهد. در میکروبیوتای روده، میکروبهایی از خانواده Bacteroidetes و Firmicutes غالب هستند در حالی که در ریه Bacteroidetes، Firmicutes و Proteobacteria غالب هستند. از نظر ردهبندی، جوامع میکروبی غالب در روده و ریه مشابه هستند. با این حال، از نظر گونه، آنها به طور قابل توجهی متفاوت هستند. به عنوان بزرگترین و متنوعترین جامعه میکروبیوم پستانداران، حدود 1014 باکتری در مجرای گوارش وجود دارد. شواهد در حال ظهور نشان دادهاند که دیسبیوسیز میکروبیوتای روده با بیماریهای مزمن در سیستم گوارش یا سایر سیستمهای بدن مرتبط است. یک جامعه میکروبی متعادل در روده اهمیت زیادی در عملکرد و سلامت ایمنی دارد. نشان داده شده است که فلور میکروبی روده از طریق یک رابطه متقابل حیاتی بین میکروبیوتای روده و ریهها، که به عنوان محور روده-ریه شناخته میشود که از طریق قسمت بالایی هر دو سیستم به هم وصل هستند و بر ایمنی ریوی تأثیر میگذارد. این محور اجازه عبور اندوتوکسینها (endotoxin)، متابولیتهای میکروبی، سیتوکینها و هورمونها به جریان خون را میدهد. نکته قابل توجه، همانطور که در شکل 1 نشان داده شده است، محور روده-ریه دو طرفه است. هنگامی که التهاب در ریه رخ میدهد، محور ریه-روده میتواند تغییراتی را در خون و میکروبیوتای روده ایجاد کند.
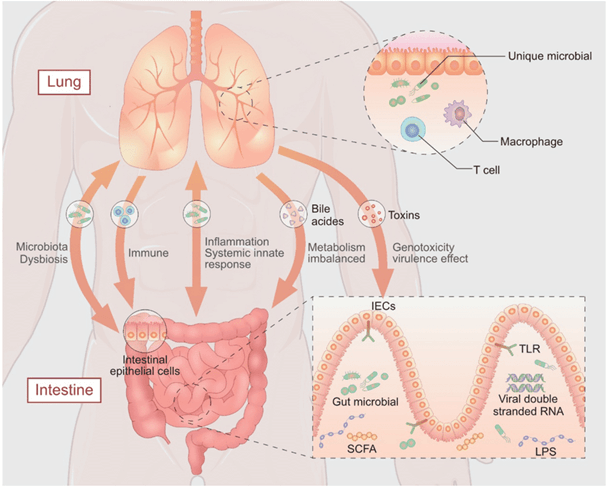
شکل 1. رابطه متقابل بین روده و ریه.
یک موضوع نوظهور مورد علاقه شدید مطالعه نقش محور روده-ریه در بیماریزایی (Pathogenesis) بیماریهای ریوی است. مطالعات فزاینده نشان داد که تغییرات در گونههای میکروبی روده و متابولیتها با تغییرات در پاسخهای ایمنی و التهاب و همچنین گسترش بیماری در ریهها مرتبط است. به عنوان مثال، خطر ابتلا به بیماری آلرژیک راه هوایی به دلیل تغییرات ناشی از آنتیبیوتیک در میکروبیوتای روده در اوایل زندگی افزایش مییابد، و درک ما از ارتباط بین میکروبیوتای روده و آلرژی راه هوایی را تسهیل میکند. مکانیسمهایی که توسط میکروبیوتای روده بر پاسخهای ایمنی و التهاب در ریهها و بالعکس تأثیر میگذارد، به طور گسترده مورد مطالعه قرار گرفتهاند. دخالت زیرمجموعههای سلول تنظیمی T و گیرندههای شبهToll (Toll-like receptors: TLRs) سیتوکینها و واسطههای التهابی، سورفکتانت (عامل فعال در سطح) پروتئینD و چندین عامل دیگر به عنوان مکانیسمهای زمینهای پیشنهاد شدهاند، اما بسیاری از جزئیات آن ناشناخته هستند. با این وجود، استراتژیهای درمانی جدیدی که دستکاری میکروبیوم روده را توسط آنتیبیوتیکها، پروبیوتیکها، پریبیوتیکها، محصولات طبیعی یا رژیمهای غذایی هدف قرار میدهند، در بیماریهای مختلف ریوی توسط مطالعات بالینی و آزمایشگاهی مورد آزمایش قرار گرفتهاند. در مقاله حاضر، نقش نوظهور محور روده-ریه را در بیماری آسم بررسی میکنیم، و در مقالات بعدی به سایر بیماریهای ریوی میپردازیم.
آسم یک بیماری مزمن تنفسی شایع است که افراد را در هر سنی تحت تأثیر قرار میدهد اما معمولاً در دوران کودکی شروع میشود. این یک بیماری پیچیده با رخنمودهای (فنوتیپهای: Phenotypes) متعدد با ویژگیهای فیزیولوژی بیماریشناسی و بالینی متفاوت است. از آنجایی که ایمنی نقش حیاتی در بیماریزایی آسم دارد، مانند دخالت زیرمجموعههای سلولهای T تنظیمی و TLRها، فرض شد که ارتباطی بین میکروبهای روده و آلرژی وجود دارد. این فرضیه به تدریج از طریق یافتن افزایش خطر ابتلا به آسم به دلیل قرار گرفتن در معرض آنتیبیوتیک در سال اول زندگی تأیید شد. تغییرات ایمنی ناشی از فلور میکروبی نشان میدهد که قرار گرفتن در معرض تغییرات میکروبی بر خطر ابتلا به آسم تأثیر میگذارد. در یک مطالعه، مشخص شد کودکان یک ساله که از مادران مبتلا به آسم با ترکیب میکروبی نابالغ متولد میشوند، در سن 5 سالگی بیشتر در معرض خطر ابتلا به آسم هستند. این یافته نشان داد که کمبود تحریک میکروبی در ابتدای زندگی ممکن است خطر آسم وراثتی را ایجاد کند و بلوغ کافی میکروبیوتای روده در این دوره ممکن است برای پیشگیری مفید باشد. تنوع کلی کم میکروبیای روده نوزاد در ماه اول زندگی با رشد آسم در کودکان 7 ساله مرتبط بود. تنوع میکروبی روده در اوایل زندگی ممکن است از التهاب راه هوایی در آسم از طریق میانجیگری تعادل Th1/Th2 جلوگیری کند.
| راجع به بیماری آسم بیشتر بدانیم. |
شواهد جدید نشان میدهد که الگوهای بلوغ میکروبیوم روده بر خطر آسم کودکان تأثیر میگذارد. در یک مطالعه، DNA باکتریایی جدا شده از نمونه مدفوع 92 کودک مبتلا به آسم و 88 کودک سالم شناسایی شدند. نتایج نشان داد که Akkermansia muciniphila و Faecalibacterium prausnitzii در گروه مبتلا به آسم نسبت به گروه سالم کاهش یافته است. هر دو گونه باکتری ممکن است التهاب را از طریق تعدیل متابولیتهای ترشح شده، مانند افزایش IL-10 و کاهش IL-12 سرکوب کنند. سطوح فاکتورهای التهابی از جمله پروتئین واکنشی C (CRP)، فاکتور نکروز تومور آلفا (TNF-α) و اینترلوکین-6 (IL-6) در سرم محیطی کودکان مبتلا به آسم به طور قابل توجهی بالاتر از گروه کنترل بود. به طور خاص، CRP با بار کلی باکتریهای روده و امتیازات مقیاس رتبه بندی علائم گوارشی (GSRS) همبستگی مثبت داشت، که نشان میدهد با افزایش سطوح فاکتورهای التهابی در سرم محیطی، احتمال عدم تعادل میکروبی روده و علائم نامتناسب دستگاه گوارش در کودکان مبتلا به آسم افزایش مییابد. علاوه بر ترکیب تغییر یافته میکروبیوتای روده، تغییر متابولیتهای مرتبط نیز مشاهده شده است. کاهش قابل توجهی در محتوای کل اسیدهای چرب و غلظت مطلق اسیدهای خاص شامل استات، بوتیرات و پروپیونات و همچنین محتوای ایزواسیدها در مدفوع بیماران مبتلا به برونکیال در مقایسه با گروه شاهد عادی مشاهده شد. الگوهای میکروبیاتای روده در بزرگسالان مبتلا به آسم نیز مورد مطالعه قرار گرفته است. در یک مطالعه آزمایشی، روابط معنیداری بین ترکیب فلور میکروبی روده، حساسیت به هوا و عملکرد ریه در بزرگسالان مبتلا به آسم و غیرآسم مشاهده شد.
با این حال، مکانیسمی که میکروبیوتای روده بر شروع و گسترش آسم تأثیر میگذارد، تا حد زیادی ناشناخته باقی مانده است. میکروبها، نمکهای صفراوی و سایر محرکهای ایمنی از دستگاه گوارش ممکن است نقش حیاتی در ایمنی مخاطی دستگاه تنفسی داشته باشند. مخاط اپیتلیال (Epithelial mucosa) و سلولهای دندریتیک (Dendritic cells) و همچنین پپتیدهای ضد میکروبی (Antimicrobial peptides) ترشح شده توسط سلولهای ایمنی عوامل اصلی در پاسخ به عوامل محیطی در راههای هوایی هستند. اپیتلیوم فعالیتهای ایمنی تنفسی موضعی را کنترل میکند که توسط لنفوپویتین استرومایی تیموس (Thymic stromal lymphopoietin)، IL-25 و IL-33 نیز انجام میشود، که ممکن است منجر به التهاب نوع Th2 شود، بنابراین ابتلا و توسعه آسم را تسهیل میکند. میکروبیوم روده به تولید لنفوسیتهای T تنظیمکننده (Treg: The regulatory T cells) کمک میکند و ریه را نسبت به آلرژنهای خوراکی مستعدتر میکند. لنفوسیتهای T تنظیمکننده ایجاد شده در محیط، که به عنوان القایی (iTreg) شناخته میشوند، عمدتاً در لکههای پیر آستر مخاطی بافت نگهدارنده رودهها (mesenteric lamina propria Peyer’s patches) و غدد لنفاوی روده کوچک و بزرگ تحریک میشوند. شواهد فزاینده حاکی از آن است که میکروبیوم روده نقش مهمی در هماهنگ کردن ایمنی ذاتی و تطبیقی که در ایجاد آسم دخیل است دارد، در حالی که مکانیسمهای مولکولی پایه نیاز به شناسایی بیشتری دارند.
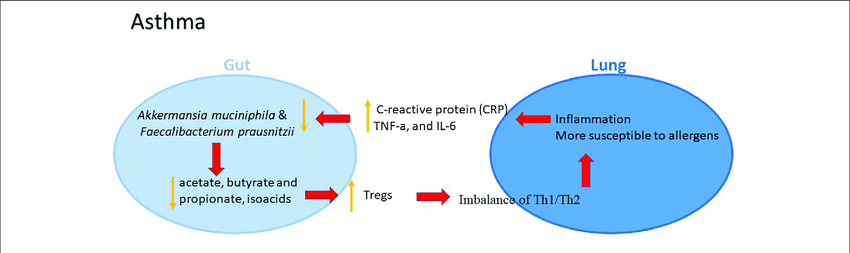
نقش بالقوه محور روده-ریه در بیماری آسم
https://www.sums.ac.ir/page-Print/fa/0/printskin-dorsaetoolsenews